z国将进一步与GUO际接轨,推进eCTD等标准应用,提高YAO品注册效率和质量。AI技术可能在YAO品注册领域广泛应用,如辅助审评人员工作。未来YAO品注册资料将更注重结构化数据,有助于监管机构GAO效获取和利用数据。eCTD等数字化工具将推动YAO品监管向智慧监管和全生命周期监管发展,提高监管效率和质量。区块链技术具有应用前景,可构建全球统一的YAO品申报数据平台。数据化时代,YAO品注册领域将更注重数据收集、分析和利用,为监管机构和企业提供决策支持。总而言之,展望未来,随着eCTD在YAO品注册领域的广泛应用和不断发展,Z国将逐步建立起与GUO际接轨的YAO品注册体系。这将有助于提高YAO品注册的效率和质量,推动YAO品走向世界舞台。同时,企业也需要密切关注技术发展动态和监管政策变化,及时调整自身战略和规划,以适应未来的市场竞争和监管要求。 中NDA注册申报相关技术支持。浦东新区赋悦科技eCTD格式
设施费动态调整 API工厂和制剂工厂年费分别约6.8万和14.5万美元(2025财年),CMO工厂费用为制剂费的24%。国外工厂需额外支付1.5万美元跨境检查费。 缴费时限与惩罚 费用需在财年首日(10月1日)起20天内缴纳,逾期将列入拖欠名单并暂停ANDA受理,涉事药品视为冒牌产品。 豁免与特殊情形 PET药物、非商业产品及停产超一年的工厂可豁免缴费。已缴费工厂若年度内无生产活动,仍需缴纳费用。 行业影响与策略 费用上涨推动企业优化申报策略,例如集中ANDA提交周期、采用CMO外包降低设施费,并通过预认证(如DMF完整性评估)减少重复支出。静安区INDeCTD递交中DMF注册申报相关技术支持。
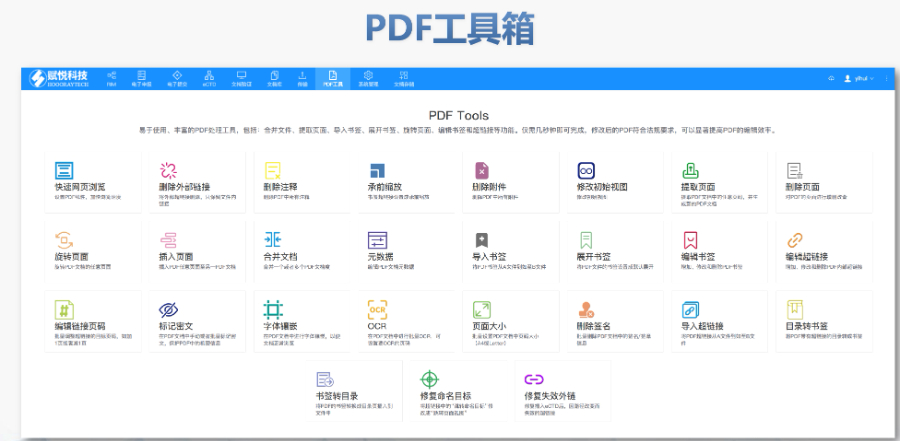
赋悦Word插件自主研发Word插件kuai速编辑:整合word常用功能按钮,避免频繁切换菜单;内置标题、段落、文字、目录、超链接等的格式和样式,可kuai速设置和更文档的格式kuai速链接:双击或者拖拽的方式,制作文本超链接或者题注超链接;可搜索全文关键字,自动制作超链接文档拆分:可根据不同的条件将word文件颗粒化,如分节符、页眉、页脚、页码范围和自定义页码等PDF转换:WORD转PDF,自动判断是否生成书签,自动镶嵌所有字体,生成PDFkuai速网页浏览的PDF,确保生成的PDF所有属性符合法规要求文档验证:验证文档的字体、字号、纸张、页面布局、空白页、页码、编号、目录、超链接等,并且可以ding位验证结果可定制:可根据用户需求定制格式和样式模板。
申报流程与要求资料准备内容要求:包括产品描述、生产工艺(原材料来源、设备参数等)、质量控Z标准(SOP、稳定性数据)、安全性与毒性研究等。格式规范:采用CTD(通用技术文件)格式,按模块分章节(如模块3为CMC数据)。电子提交需符合eCTD标准(文件小于10GB通过ESG系统提交,超过可选用CD-ROM)。提交与注册预分配DMF号:需在提交前申请,确保文件与编号绑定。授权书(LOA):需向引用DMF的制剂厂商提供授权信,明确可查阅的章节。费用:Ⅱ类原料DMF需缴纳年费(2024年约9,468美元)。FDA审核流程行政审评:2-3周内确认文件完整性。完整性审评(CA):针对Ⅱ类DMF,约60天。技术审评:在DMF被制剂申请(如ANDA、NDA)引用时启动,周期60-180天。结果反馈:FDA可能要求补充数据,但DMF本身无“批准”状态,通过后可能收到“无进一步意见函”(NoFurtherCommentLetter)。 美国注册邓白氏号申请相关技术支持。
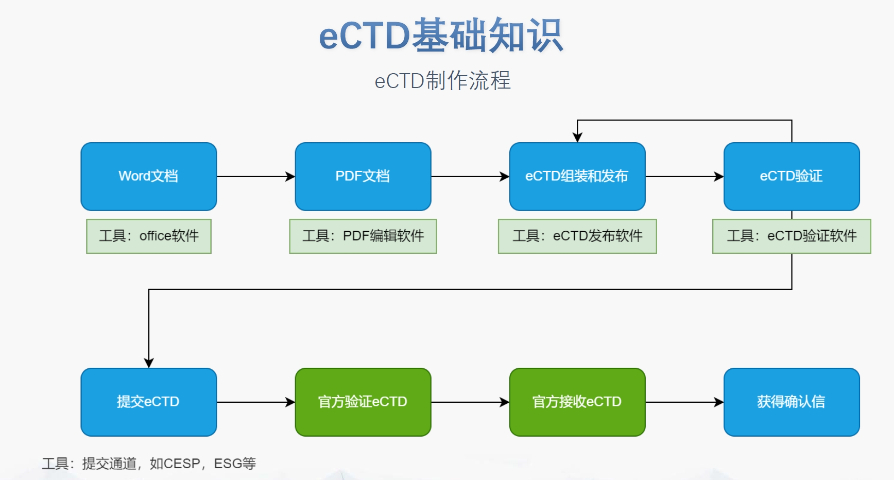
GDUFAIII框架与费用分类2022年更的GDUFAIII将费用分为ANDA申请费、DMF认证费、项目费及设施费四类,实施周期至2027年。2025财年ANDA费用长至约22万美元,较2024年增幅达,反映审评成本上升。ANDA申请费规则费用需在提交时缴纳,若申请被拒可退还75%。重提交视为申请,需再次缴费。关联API的工厂数量影响总费用,例如某ANDA引用3个API且涉及6家工厂,需支付6倍DMF费用。DMF费用机制II类原料yaoDMF需在引用前缴费,一次性支付约(2025财年)。未缴费DMF不得用于支持ANDA,否则触发退审。项目费分级管理根据企业获批ANDA数量分为大、中、小型三级,2025年大型企业年费约34万美元。附属公司ANDA数量合并计算,缴费责任可由母公司或任一附属公司承担。 瑞士IND注册申报相关技术支持。杭州INDeCTD软件
美国API的DMF申报相关技术支持。浦东新区赋悦科技eCTD格式
文件生命周期管理:eCTD支持文件替换(Replace)、删除(Delete)等操作,而非增文件。例如,更临床研究方案时需用Replace操作覆盖旧版本。基线提交(BaselineSubmission)可用于补充历史纸质资料,但需在封面函中声明无内容变更。临床数据与研究标签文件(STF):模块4和5中的研究数据需通过STF(StudyTaggingFiles)引用,确保数据与文档关联。FDA要求数据集(如SASXPORT格式)能置于模块3-5,且单个文件超过4GB需拆分。2022年统计显示,58%的ANDA因研究数据技术拒绝标准(TRC)错误被拒。电子签名与表格要求:FDA表格(如356h、1571)需使用数字签名,PDF文件禁止加密或设置编辑限制。电子签名需符合21CFRPart11规范,确保身份验证、不可否认性和数据完整性。外包服务与系统解决方案:赋悦科技累计提交超2000份eCTD申请,外包可降低40%人工错误率。浦东新区赋悦科技eCTD格式