- 品牌
- 有梦生物
- 服务项目
- 切片染色
返蓝是通过碱性环境(pH 7.0-8.0)使苏木精染料发生色相转变的重要步骤。分化后的切片在酸性条件下呈红褐色,经温水(约50℃)或弱碱性溶液(如0.1%氨水、Scott蓝化液或自来水)处理后,染料分子结构重组,细胞核恢复为稳定的蓝紫色。返蓝时间通常为5-15分钟,需根据切片厚度和组织类型调整:较厚切片或富含细胞核的组织(如淋巴结)需延长返蓝时间;而薄切片或细胞稀疏组织(如脂肪)则可适当缩短。值得注意的是,自来水返蓝可能因水质硬度差异影响效果,建议使用pH缓冲液确保稳定性。整个过程需避免剧烈晃动,防止组织脱片,同时保持溶液清洁,避免沉淀物附着影响观察。钙染色如茜素红法可检测组织内微小钙化,对甲状腺髓样*或乳腺导管内*的诊断具有提示意义。西藏血管病理切片
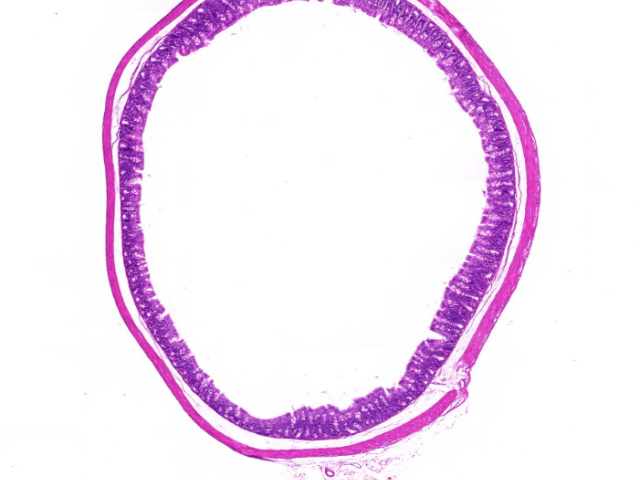
近年来,随着分子病理学和人工智能技术的深度融合,病理切片染色技术正经历**性变革。多重免疫荧光染色(mIHC/mIF)通过光谱分离技术(如Opal 7色系统)可在单张切片上同步检测PD-L1/CD8/FOXP3等7种标志物,结合多光谱成像系统(如Vectra Polaris)实现**微环境免疫细胞亚群的精确定量,其空间分辨率可达0.25μm/pixel,较传统IHC诊断效率提升5倍以上。数字病理与AI分析已进入临床实用阶段,如谷歌DeepMind开发的乳腺*淋巴结转移检测系统(灵敏度达99.3%),可对全切片图像(WSI)进行实时分析,自动标注可疑区域并生成结构化报告。西藏血管病理切片纳米金标记技术通过表面等离子共振增强信号,显著提高原位杂交检测的灵敏度和分辨率。
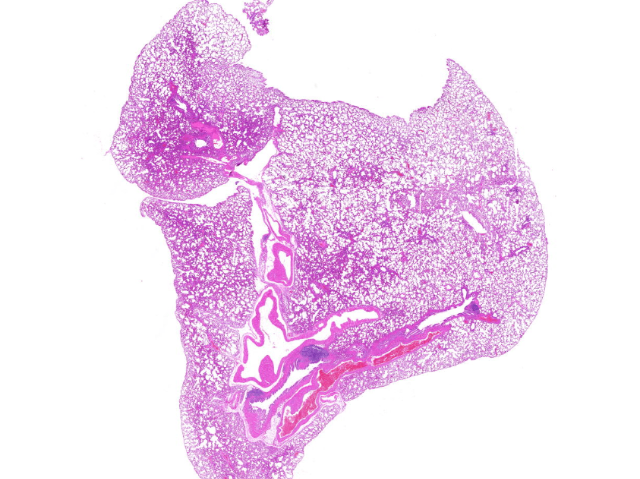
免疫荧光染色(Immunofluorescence Staining, IF)是结合免疫学特异性和荧光检测灵敏度的先进技术,其**原理是利用荧光素标记的抗体(如FITC发绿光、Cy3发红光)与靶抗原的特异性结合。标准操作流程包括:新鲜冰冻切片或细胞爬片经**/甲醇固定后,用0.1% Triton X-100通透处理5分钟;随后以5%BSA封闭30分钟减少非特异性结合;滴加一抗(如抗dsDNA抗体1:50稀释)湿盒内37℃孵育1小时;PBS洗涤后与荧光二抗(如Alexa Fluor 488标记羊抗人IgG)避光孵育45分钟;***用含DAPI的抗淬灭封片剂封片,荧光显微镜观察。
数字化病理技术的快速发展为组织染色质量的客观评估提供了高效、标准化的解决方案。借助专业图像分析软件(如Aperio ImageScope、HALO等),研究人员能够对染色切片进行自动化定量评估,大幅提升分析效率和准确性。这些软件系统通常采用多维度的评估指标:核质对比度通过计算苏木素(细胞核)和伊红(细胞质)的灰度值差异来量化染**分度;染色均匀性则利用统计学方法(如像素强度的标准差分析)评估整张切片的染色一致性;阳性信号面积比例通过智能阈值分割技术精确识别目标染**域(如免疫组化的棕褐色阳性信号),并计算其占组织总面积的比例;背景噪声水平则采用信噪比分析来鉴别有效信号与非特异性染色。相较于传统人工评估,自动化分析不仅避免了主观偏差,还能同时处理大批量切片数据,显著提高筛查效率。此外,数字化评估可生成标准化报告,便于不同实验室间的数据比对和质量控制,为精细医学研究和临床病理诊断提供可靠的技术支持。刚果红染色在淀粉样变性诊断中具有特异性,偏振光下呈现苹果绿双折光可作为确诊的重要依据。
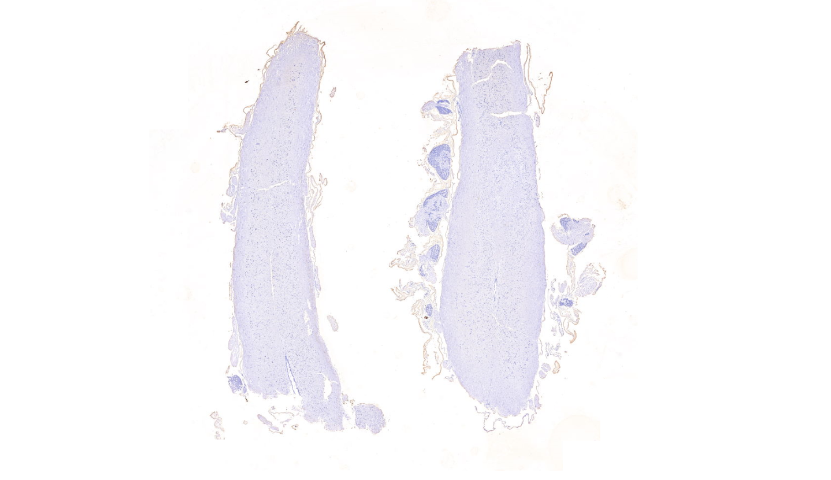
病理切片染色质量是确保诊断准确性的基石.,需建立覆盖全流程的标准化质控体系。在切片制备阶段.,厚度控制需采用高精度切片机.(如徠卡RM2255)配合厚度校准片验证,确保3-5μm标准.(胰腺等致密组织可薄至2μm,脂肪组织不超过6μm)。.染色过程质控应执行双人核对制度:①HE染色需监控苏木精染液氧化程度.(每日测OD值维持在0.8-1.2),.②IHC染色每批次必须运行阴阳性对照片.(如乳腺*组织芯片包含ER/PR/HER2梯度表达样本)。.铁染色(普鲁士蓝反应)可检测组织内铁沉积,为血色病或慢性溶血性贫血提供病理学证据。西藏血管病理切片
番红O-固绿染色可区分软骨与骨组织,在骨关节炎或骨**的病理评估中提供重要信息。西藏血管病理切片
特殊组织处理技巧:对易脱片的脑组织,可在染色前用1%多聚赖氨酸处理载玻片***斑块建议先进行苏木精复染(30秒),再油红O染色以显示泡沫细胞定位染色失败补救:对已脱水的切片可用70℃热PBS处理2分钟恢复脂质显色***研究显示,联合尼罗红荧光染色(Ex/Em=488/525nm)可提高微小脂滴(<1μm)的检出率,尤其适用于非酒精性脂肪肝的早期诊断。实验室应建立标准操作手册,明确规定从取材到封片的全流程时间控制(总时长不超过45分钟),确保染色结果的可重复性。西藏血管病理切片
- 西藏血管病理切片 2026-03-17
- 海南脑组织病理切片销售电话 2026-03-16
- 江西肝脏病理切片怎么样 2026-03-16
- 湖南哪里有病理切片怎么样 2026-03-16
- 湖北哪里有病理切片销售 2026-03-11
- 重庆脾病理切片销售 2026-03-11
- 广西脾病理切片销售 2026-03-10
- 江西心脏病理切片服务电话 2026-03-10
- 贵州哪里有病理切片实验效果 2026-03-09
- 广东病理切片24小时服务 2026-03-09
- 上海病理切片销售价格 2026-03-06
- 湖南脾病理切片 2026-03-05

