临床前动物实验推荐南京英瀚斯生物。,常规流程上,疫苗研发从细胞水平的体外实验、到临床前动物实验,再到人体临床试验,是一个漫长的过程。证明疫苗安全有效的过程非常缓慢,从少数人的临床试验,只是观察免疫反应副作用等,到需要成千上万人来测试疫苗效果的大型试验,这一过程至少需要1年时间。与动物疫苗在实验室获得结果不同,评价人的疫苗有效性依赖于长时间的统计数据,我们需要在一定时间内监测注射疫苗者与注射安慰剂者的***率的差别,而在这个过程中,通常还会有各种影响因素干扰结果,这也就是疫苗进程**拉长的原因。实验过程中需严格控制变量,确保数据的可靠性。北京专注临床前动物实验价格
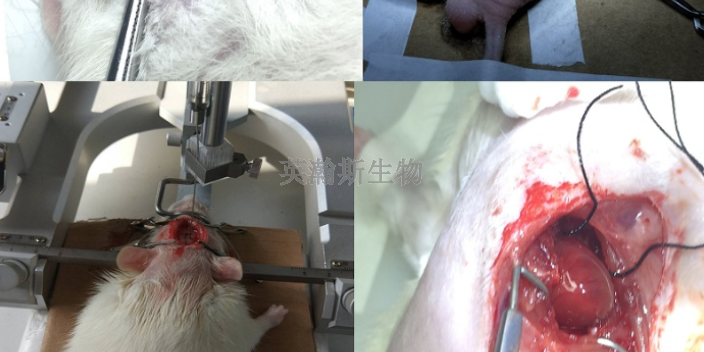
申请人应尽临床前动物实验的可能通过初步研究(如实验室研究等)来验证所确定的风险控制措施的有效性,只有在实验室研究不足时,才能通过动物实验进行进一步验证。动物实验数据可作为风险/收益分析的支持数据。1.可行性研究:可行性研究是指在产品设计和开发阶段,为确认/验证产品的工作原理、作用机理、设计、可操作性、功能性、安全性等方面,或识别新的意外风险而进行的研究。2.安全性研究:申请人采取风险控制措施后,可通过动物实验对部分产品的安全性进行适当评价。3.有效性研究:尽管某些医疗器械在动物和人类之间的有效性可能存在一些差异,但合理设计的动物实验可以支持产品的有效性(包括性能和操作)。新疆靠谱临床前动物实验价格临床前动物实验需遵循动物伦理与实验规范。
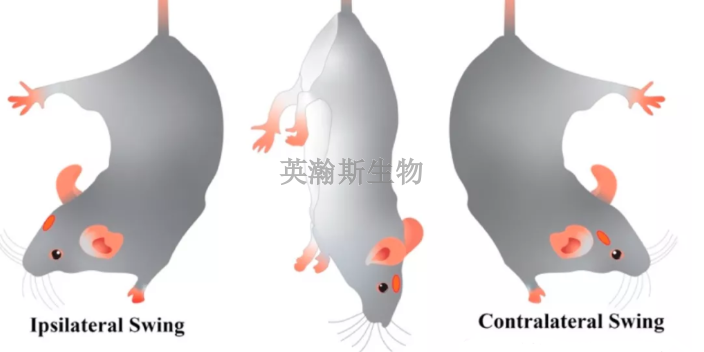
临床前动物实验除了《药物非临床研究质量管理规范》第十八条对受试物和对照品的使用和管理的基本要求之外,鉴于医疗器械的受试物多为固体材料或器械,建议普遍表征研究中使用的所有受试物和对照品。由于不断的工艺改进和优化,委托方可能在开始临床研究之前研发多次重复的受试物,因此建议在关键的临床前动物实验研究使用**比较终临床设计的受试物。如果没有使用比较终设计的受试物,应确定比较终的临床设计样品与动物实验研究的设计相比,对患者没有新的风险。建议将受试物和对照品包装、消毒,并以与临床产品相同的方式运送到研究现场。应开发一种从采购到使用过程中全程追踪试验器械和对照器械的方法。
临床前动物实验的要求(1)从事药物研究开发的机构的要求。应当具有与试验研究项目相适应的人员、场地、设备、仪器和管理制度;所用试验动物、试剂和原材料应当符合国家有关规定和要求;并应当保证所有试验数据和资料的真实性。(2)研究用原料药的规定。单独申请注册药物制剂的,研究用原料药必须具有药品批准文号、《进口药品注册证》或者《医药产品注册证》,该原料药必须通过合法的途径获得。(3)境外药物试验研究资料的处理。药品注册申报资料中有境外药物研究机构提供的药物试验研究资料的,必须附有境外药物研究机构出具的其所提供资料的项目、页码的情况说明和证明该机构已在境外合法登记的经公证的证明文件,并经国家食品药品监督管理局认可后,方可作为药品注册申请的申报资料。国家食品药品监督管理局根据审查需要组织进行现场核查。临床前动物实验包括药代动力学和毒理学研究。
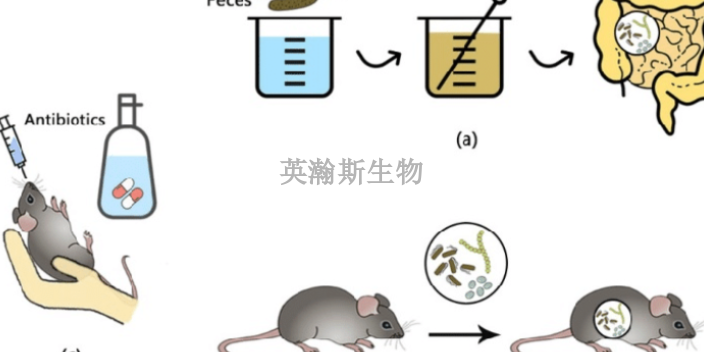
从微生物产物中发现和研制抗*****,是极其复杂的、综合性极强的工作,被称为“一条龙”,大致可分为五部分:①获得产生菌:从全国各地采集的土壤样本中,培养、分离数以千计的菌株。②制备发酵液样品:将各种各样的菌种进行培养发酵,取得为数众多的发酵液样品。③初筛检测:对大量的发酵液样品进行筛选,检出有潜在抗**活性的样品。④提取纯化:对初筛阳性发酵液样品中的有效物质,进行提取与纯化。⑤临床前动物实验疗效评价:利用实验动物**模型,观察提取物的疗效。临床前动物实验能够模拟药物在人体内的代谢过程。黑龙江值得信赖临床前动物实验评价
生物药临床前动物实验指标。北京专注临床前动物实验价格
我国医疗器械临床前安全性评价还没有实施GLP管理,但要求开展医疗器械生物学评价试验机构需要具备中国合格评定国家认可委员会(ChinaNationalAccreditationServiceforConformityAssessment,CNAS)及中国计量认证(ChinaMetrologyAccreditation,CMA)认可的实验室资质,而对开展临床前动物实验研究还没有明确的资质要求。GLP管理与CNAS认证体系虽然是两个不同的质量管理体系,但基本内容有很多的相同性和相似性。如果参照我国相关医疗器械动物实验研究指导原则和国家或行业标准,在具备CNAS及CMA认可资质的实验室质量管理体系下开展医疗器械临床前动物实验研究,可以基本满足临床前动物实验研究质量管理要求。北京专注临床前动物实验价格