外泌体的研究和应用离不开其高效的分离与纯化技术。由于外泌体的尺寸较小且在生物体液中的浓度较低,如何从复杂的生物样本中高效、准确地提取外泌体是当前面临的一个技术难题。常用的分离方法包括超速离心法、免疫亲和捕获法、纳米颗粒过滤法以及基于聚合物的沉淀法等。其中,超速离心法是最常见的方法,但其操作繁琐且需要较长时间。此外,免疫亲和捕获法通过特定的抗体识别外泌体表面特征分子,能够较为精细地分离目标外泌体。随着纳米技术的发展,越来越多的新的分离技术也被提出,如微流控芯片技术、磁性纳米粒子法等。这些新兴技术有望提高外泌体分离的效率和纯度,为后续的研究和临床应用提供更加可靠的工具。外泌体检测,外泌体检测服务,医学科研实验服务。辽宁专门做外泌体粒径分析
外泌体的产生过程为:细胞膜内陷,形成内体(endosome),再形成多泡体(multivesicularbodies,MVB),比较后分泌到胞外成为外泌体。外泌体中携带有母细胞的多种蛋白质、脂类、DNA和RNA等重要信息。外泌体比较早见于1981年,EGTrams等在体外培养的绵羊红细胞上清液中发现了有膜结构的小囊泡,并命名为exosome。对于外泌体的作用,当时推测为细胞排泄废物的一种方式。1996年GRaposo等发现类似于B淋巴细胞的免疫细胞也会分泌抗原呈递外泌体(antigenpresentingvesicle),所分泌的外泌体可以直接刺激效应CD4+细胞的抗**反应。2007年HValadi等进一步发现细胞之间可以通过外泌体中RNA交换遗传物质。随着有关外泌体研究越来越多,研究者发现它普遍参与了机体免疫应答、抗原呈递、细胞分化、**生长于侵袭等各种生物过程中。天津外泌体粒径分析外泌体检测服务,一站式生物外泌体检测服务平台。
外泌体的提取方法有多种:包括传统的差速离心、密度梯度离心,以及后来发展的超滤法、聚合物沉淀法、免疫分离、隔离筛选法、体积排阻色谱法等。这些方法各有利弊。外泌体经细胞分泌后存在于体液或者血液中,故检测外泌体的样本一般为血液(全血、血浆)、体液(尿液、唾液、脑脊液、羊水、唾液等)、细胞上清液。提取所需要样本量血清:样本量>5ml(全血10ml)。血浆:样本量>5ml(全血10ml)。体液:样本量>20ml。细胞培养上清液:样本量>20ml。
外泌体和微囊泡的区别在于其生成的方式不同。从晚期内体来源产生的细胞外囊泡称为外泌体,从细胞膜直接出芽产生的细胞外囊泡称为微囊泡。二者的大小也有所不同,外泌体的粒子直径在40~100nm范围,微囊泡的粒子直径在100~1,000nm,但有报道发现也存在直径较小的微囊泡,所以无法明确从粒子大小来区分二者。外泌体是健康细胞和*细胞均可释放的小膜泡,***存在于人体的血液、乳汁、尿液以及唾液等多种体液中,其种类和数量与机体的生理状态息息相关。如果选择一家靠谱的外泌体检测服务公司。
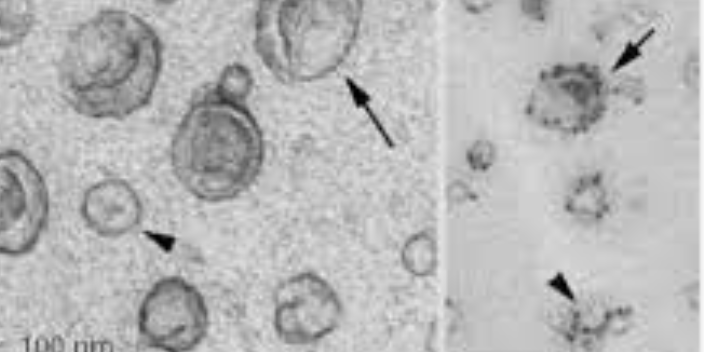
外泌体鉴定透射电镜观察能够确认外泌体的形态学特征,但无法体现样本中所有外泌体颗粒的粒径分布情况及整体浓度;流式细胞仪可测定的粒径大小为150nm以上,并不适合检测游离的外泌体颗粒。英瀚斯生物采用基于马尔文Nanosight平台的纳米颗粒追踪分析 (Nanoparticle Tracking Analysis, NTA) 技术,快速、精细地分析外泌体粒径分布浓度,为外泌体存在提供有力证据。目前外泌体的提取方法主要可归纳为以下六种:一是超速离心法;二是过滤离心;三是密度梯度离心法;四是免疫磁珠法;五是PS亲和法;六是色谱法。外泌体组学_外泌体测序 南京英瀚斯生物。辽宁专门做外泌体粒径分析
外泌体检测服务-实验外包检测。辽宁专门做外泌体粒径分析
外泌体没有限定单一的分离手段,多种手段都可以进行细胞外囊泡的富集。《指导要求》编写者们认为“高回收率,低特异性”的富集手段是指那些富集囊泡的同时会有大量的非囊泡组分被富集,甚至细胞的整个分泌组都会被掺入其中,归入这一类的分离手段主要包括通过改变电荷或通过高聚物作用的沉淀试剂盒、低分子量截流的超滤分离、超长时间和超高离心力的超速离心等。 目前较常用的外泌体提取方法是differential centrifugation (DC)——差速离心法。也有用试剂盒提取外泌体,但效率均不高。辽宁专门做外泌体粒径分析