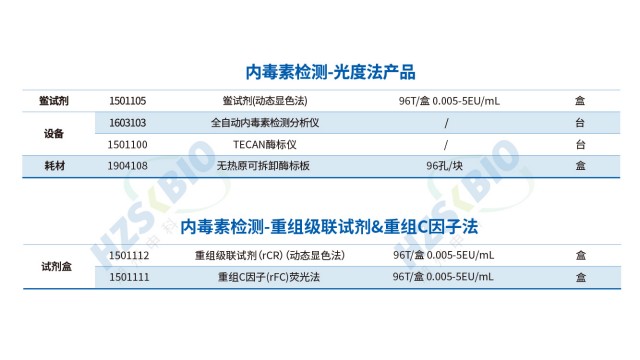
鲎试验法(LAL 法)是细菌内毒素检测的经典方法,依据反应监测方式可分为三类:凝胶法、浊度法和显色法。凝胶法通过观察是否形成凝胶判断内毒素是否超标,其优势是操作简便、成本较低,适用于定性或半定量检测,如医疗器械初筛;浊度法通过监测反应体系浊度变化速率定量内毒素,灵敏度高(可达 0.005 EU/mL),适用于生物制品原液等高精度需求场景;显色法基于显色底物的吸光度变化定量,抗干扰能力较强,适配复杂基质样品(如含蛋白质的注射液)。三种方法均需严格控制反应温度(37℃±1℃)和时间,确保结果可靠性。
内毒素检测方法多样,影响因素及实验干扰较多,包括实验操作步骤、样品处理等方面。江苏抗体药物内毒素检测技术服务
湖州申科生物细菌内毒素工作标准品(CSE)源自大肠杆菌(E.coli O111:B4),经过提取精制获得脂多糖,并以细菌内毒素国家标准品为基准标定效价,每支效价处于 10 - 100EU ,量值准确且可靠。在工业内毒素检测中,该标准品应用广且关键。首先,能用于鲎试剂灵敏度复核实验,帮助检测人员准确确认鲎试剂对细菌内毒素的敏感程度,保障检测方法的有效性;其次,可开展干扰试验,评估样品中可能存在的干扰物质对检测结果的影响,以便优化检测流程和方法;再者,能充当各种阳性对照,为检测过程提供参照,确保检测结果的准确性与可靠性。这款标准品不仅适用于凝胶法鲎试剂系列实验,在光度法鲎试剂系列实验中同样能发挥重要作用。使用时,只需参照中国药典2025版第四部通则 1143 的相关介绍进行操作即可。凭借效价标定准确和适用性的优势,该标准品为生物制品、化学药品等各类样品的细菌内毒素检测提供了稳定且可靠的标准,助力企业和检测机构严格把控产品质量,满足法规要求。
北京生物制品内毒素检测技术升级重组级联试剂(rCR)推动内毒素检测向可持续发展转型,兼顾生态保护与药品安全质控。
内毒素检测结果误差可能源于多环节:试剂方面,鲎试剂(LAL )或试剂批间差异、过期试剂活性下降会导致结果偏差,需通过试剂验收(如阳性对照回收率验证)确保质量;操作方面,实验器具未除热原(如玻璃器皿未干热灭菌)、加样体积不准确会引入污染或误差,需严格执行 SOP(如器皿 250℃干热灭菌≥30 分钟);环境方面,实验室空气中的微生物孢子、粉尘可能污染样品,需在洁净工作台操作并设置阴性对照。此外,反应温度波动(偏离 37℃±1℃)会影响酶活性,需使用恒温孵育器精确控温,确保反应条件稳定。
β- 葡聚糖是鲎试剂(LAL)检测内毒素的常见干扰物,可活化 LAL 中的 G 因子通路,导致假阳性结果。干扰多见于含植物源原料的样品(如中药注射剂)、生物发酵产物或环境真菌污染的样品。消除方法包括:使用特异性 LAL 试剂(如添加葡聚糖抑制剂的 LAL),其只对内毒素敏感而不受 β- 葡聚糖影响;采用加热处理(如 80℃加热 10 分钟)破坏 β- 葡聚糖结构;或通过亲和层析去除样品中的 β- 葡聚糖。检测时需设置 β- 葡聚糖阳性对照,若对照反应阳性而内毒素标准品无反应,表明存在干扰,需优化前处理步骤后重新检测。
细菌内毒素试验(BET)是用鲎变形细胞裂解物(LAL)测内毒素的体外方法,LAL 测试获国际药典推荐。
在为新物料或新产品、中间产品建立细菌内毒素检测方法时,常会遇到各种困难,尤其是尚处于新药研发早期阶段的药物。此时,由于药物制剂、缓冲系统等还不稳定,经常会发生变化,这样就给方法的建立带来了不同程度的影响。在建立细菌内毒素检查法之前,须尽可能多地了解有关该药品的基本信息,例如:有关样品的可溶性信息、推荐的稀释液、在水中的溶解度以及合适溶剂,样品的pH范围,分子量大小;如果是蛋白产品,还要了解该产品的等电点,产品规格、体积或重量,拟用于临床的用法和用量等,以便选择合适的样品处理方法和内毒素检测方法。
湖州申科内毒素检测服务含低内毒素回收,通过不同样品前处理方式搭配多种检测方法,较大程度解决LER问题。江苏医疗器械内毒素检测操作步骤
细菌内毒素工作标准品可用于鲎试剂灵敏度复核、干扰试验,适配凝胶法与光度法实验。江苏抗体药物内毒素检测技术服务
湖州申科生物重组级联试剂(rCR)采用基因工程技术合成,完全模拟了天然鲎试剂中的酶促级联放大反应。重组鲎试剂反应体系中包含重组C因子、重组B因子和重组凝固酶原。当供试品中存在内毒素,重组C因子识别内毒素后活化,会依次级联活化下游重组B因子和重组凝固酶原。凝固酶原转化为具有生物活性的凝固酶后,识别并催化下游带显色基团的底物产生显色反应。显色反应的强度和内毒素浓度成正相关,从而定量检测内毒素。本产品用于定量测定人用和动物用注射药物、生物制品及医疗器械等样品中的细菌内毒素的含量。
江苏抗体药物内毒素检测技术服务