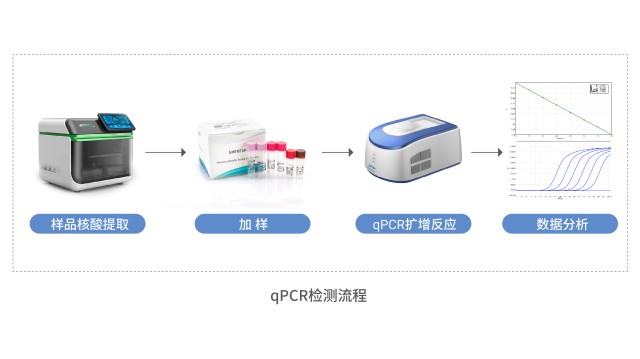
SHENTEK® Sf9&AcNPV 残留 DNA 检测试剂盒(多重 PCR - 荧光探针法),可对昆虫细胞(Sf9)杆状病毒表达系统所生产的基因工程疫苗中,残留的 Sf9 细胞 DNA 与杆状病毒(AcNPV)DNA 进行定量检测。该试剂盒依托 Taqman 探针原理,结合多重 qPCR 技术实现对样品中 Sf9 及 AcNPV 残留 DNA 的定量,不仅检测效率高、专一性突出,且性能稳定可靠,检测限可达到 50 copies / 反应,试剂盒还配套提供 Sf9&AcNPV 定量参考品。此试剂盒与 SHENTEK® 宿主细胞残留 DNA 样本前处理试剂盒搭配使用,能够准确定量样品中残留的 Sf9&AcNPV 微量 DNA,保障检测结果的准确性与可靠性。
湖州申科生物rHCDpurify前处理系统搭配系列宿主细胞残留DNA检测试剂盒,减少手动操作误差。云南宿主细胞残留DNA检测生产企业
宿主细胞残留DNA检测体系(qPCR法)的技术关键点涉及多个维度。1、靶标序列的查找与确定:需参照宿主物种的基因组序列,筛选出物种特异性强、高度重复且呈散在分布的序列,将其作为检测靶标。2、检测体系建立与方法验证:在适宜位点设计引物与探针,选择适配的荧光及淬灭基团。3、基于qPCR法优化体系组分比例,制备用于微量DNA模板检测的MIX,同时对线性范围、专属性等多项指标开展验证。4、检测体系稳定性保障:需完成参考品的准确标定,同时严格控制试剂批间差异,确保检测体系的稳定性。5、适配的残留DNA提取体系:需搭配合适的宿主细胞残留DNA提取体系,以应对不同样品基质的影响,实现微量残留DNA的回收提取与纯化。
四川E.coli宿主细胞残留DNA检测生产企业在CGT领域,对干细胞等产品检测残留 DNA,确保质量可控并符合监管要求。
更换宿主细胞残留DNA(HCD)检测试剂盒时,需开展一系列验证相关考量。首先参照《已上市生物制品药学变更研究技术指导原则(试行)》,根据变更对生物制品安全性、有效性及质量可控性的风险影响程度分类,实施变更前需开展充分研究与验证。其次进行全面性能验证,采用药典方法或已验证的检测方法,证明变更后分析方法与原方法等效或更优。随后开展样品检验,对比试剂盒更换前后的产品质量数据并综合评估,结合稳定性研究进行稳定性可比性分析,检测细微差异以评价变更对产品质量的影响。完成上述步骤后,再办理试剂盒更换备案;若变更后方法与原方法相当或更优,根据待检样品为原液或制剂,将变更归为中等或微小变更,微小变更可在中等变更申请中一并说明。
湖州申科生物的产品研发与制造过程遵循 ISO13485 质量管理体系要求开展,并参照 CDE《生物制品质量控制分析方法验证技术审评一般原则》、《中国药典》9101 分析方法验证指导原则及 ICH Q2 (R2)《分析方法验证指导原则》等法规文件,对 SHENTEK 系列宿主细胞残留检测试剂盒实施了全面性能验证,涵盖线性、范围、准确性、定量限、精密度、耐用性、专属性等项目,结果符合法规标准。公司可向用户提供试剂盒的详细验证报告,用户若采用此验证报告,只需开展针对样品的适用性验证(含精密度实验与回收率实验)即可。
宿主细胞残留DNA检测磁珠法自动化提取实现高通量样品处理,提升效率。
湖州申科生物动物源性生物材料残留DNA提取试剂盒(磁珠法),可对各类动物源性生物材料中的微量动物源DNA进行提取纯化。该试剂盒适配多种生物材料类型(如生物修复膜、生物补片、脱细胞基质等),能有效提取纯化微量DNA,可用于DNA荧光染料法或qPCR方法检测。此外,该试剂盒借助rHCDpurify®前处理系统可实现样品自动处理,系统内置对应处理程序,一键操作即可完成前处理。同时,该试剂盒可与SHENTEK®猪源/牛源DNA检测试剂盒搭配使用,实现对各类生物材料中猪源/牛源DNA的定量检测。
样本核酸处理、试剂盒及检测系统共同决定宿主细胞残留 DNA 检测稳定性。疫苗宿主细胞残留DNA检测
SHENTEK-96S PCR仪配套使用湖州申科各类核酸检测试剂盒,稳定实现生物制品质量检测。云南宿主细胞残留DNA检测生产企业
宿主细胞残留DNA的潜在风险中,传播性是其中一项。该风险源于残留DNA可能携带带有潜在入侵能力的完整或部分病毒基因组序列,这类序列主要有两大来源:1)整合到宿主基因组中的DNA病毒序列,或是染色体外的游离病毒DNA(例如部分疱疹病毒);2)整合入宿主基因组的反转录病毒前病毒DNA。研究显示,这类病毒DNA在适宜条件下,无论处于体外培养系统还是体内环境,都能侵入宿主细胞,或触发后续病毒生命周期环节(包括复制),存在引发病毒相关疾病的潜在威胁(尽管风险概率随生产工艺控制而明显降低)。
云南宿主细胞残留DNA检测生产企业