- 产地
- 苏州
- 品牌
- 外泌体提取试剂
- 型号
- 齐全
- 是否定制
- 是
外泌体表面有其特异性标记物(如CD63、CD9蛋白),用包被抗标记物抗体的磁珠与外泌体囊泡孵育后结合,即可将外泌体吸附并分离出来。磁珠法具有特异性高、操作简便、不影响外泌体形态完整等优点,但是效率低,外泌体生物活性易受pH和盐浓度影响,不利于下游实验,难以普遍普及。聚乙二醇(PEG)可与疏水性蛋白和脂质分子结合共沉淀,早先应用于从血清等样本中收集菌类,现在也被用来沉淀外泌体,其原理可能与竞争性结合游离水分子有关。利用PEG沉淀外泌体存在不少问题:比如纯度和回收率低,杂蛋白较多(假阳性),颗粒大小不均一,产生难以去除的聚合物,机械力或者吐温-20等化学添加物将会破坏外泌体等,因此发表文章时易受质疑。如纯度和回收率低,杂蛋白较多(假阳性),颗粒大小不均一,产生难以去除的聚合物。将人尿液来源细胞的培养基通过0.22微米滤膜过滤,以去除大的细胞残片以及其它杂质。南京外泌体提取试剂供应商
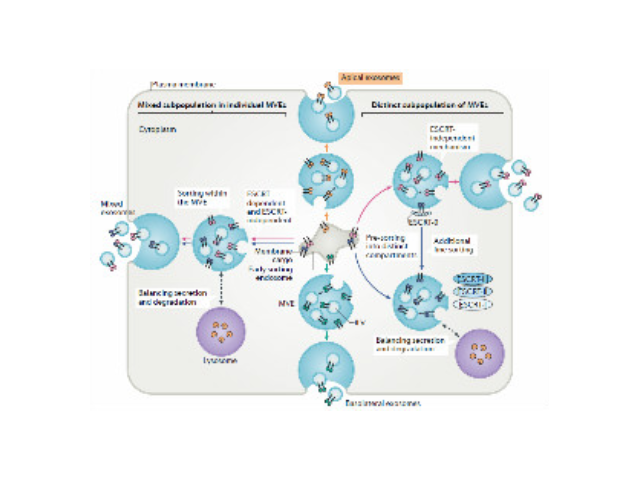
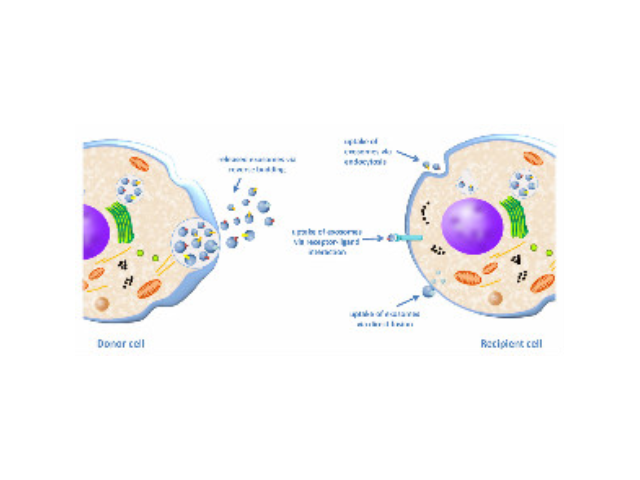
人体几乎所有类型的细胞都能分泌外泌体,外泌体普遍存在并分布于各种体液中,携带多种蛋白质、mRNA、miRNA和脂质类物质等,作为重要的传递信号分子,形成了一种全新的细胞-细胞间信息传递系统,可参与细胞通讯、细胞迁移、血管新生和一些病症细胞生长等过程。外泌体与微泡:我们知道,细胞间相互作用可以通过释放蛋白质、核酸、脂质等分子到胞外与受体结合从而介导胞内细胞传导。除此之外,细胞还可以释放膜囊泡,外泌体与微泡就是其中两种,二者相似但形成方式不同:外泌体是细胞内内溶酶体微粒内陷形成的多囊泡体,经多囊泡体外膜与细胞膜融合后释放到胞外基质中的膜囊泡,而微泡则是细胞出芽与细胞膜融合后直接脱落形成的囊泡,且外泌体大小均一,直径在40~100nm,其大小取决于其起源部位以及细胞中的脂质双层结构;而微泡大小不一,直径在50~1000nm之间。唐山正规外泌体提取试剂产品介绍在超速离心力作用下,使蔗糖溶液形成从低到高连续分布的密度阶层,是一种区带分离法。无锡正规外泌体提取试剂报价外泌体提取:高速离心沉淀外泌体。

外泌体是一种存在于细胞外的多囊泡体,可通过细胞内吞泡膜向内凹陷形成多泡内涵体,内涵体与细胞膜融合后释放其中的小囊泡。外泌体的直径在40-110nm之间,其中包含RNA、蛋白质、microRNA等多种物质,存在于血液、唾液、尿液、脑脊液和母乳等多种体液中。外泌体从发现至今已有30多年的历史,虽然较初被认为可能是细胞的“垃圾”,所以才被排出来,但是近年来研究表明外泌体具有功能活性并可进行细胞间信息传递。如今,研究已经发现外泌体在抗原提呈细胞中呈递抗原程中、一些病症细胞发生的发展、神经细胞信号转导过程中都发挥着重要作用。利用化合物沉淀将法外泌体沉淀出来。
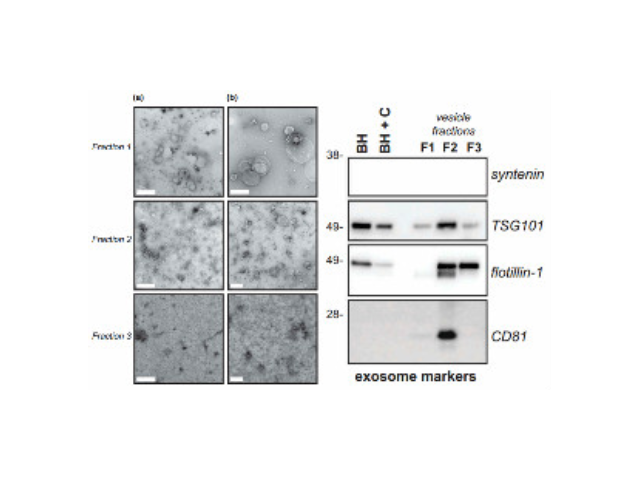
外泌体相关蛋白质与肺病的诊断:近年来众多文献报道,肺病细胞分泌的外泌体中富含多种蛋白质并促进肺病的发生的发展,是早期诊断肺病的有效途径。有研究发现,NSCLC患者肺组织外泌体表面EGFR免疫染色呈阳性的占80%,而慢性肺炎组织的外泌体EGFR呈阳性的只占2%,因而认为外泌体的EGFR蛋白可以用作NSCLC与慢性肺炎鉴别诊断的生物标志物。Park等通过Sys-BodyFlu-id数据库分析发现153种特异性胸腔积液外泌体蛋白质,进一步的Westernblotting分析显示多种特异性胸腔积液外泌体蛋白参与EGFR信号传导途径以促进一些病症的发生的发展,因此外泌体蛋白可能作为肺病诊断筛查的生物学标记物。近几年来,市场上已出现各种商业化的外泌体提取试剂盒。近年来,随着人们对外泌体的研究和认识加深。

外泌体提取:尺寸排阻色谱。尺寸排阻色谱(Size-exclusionchromatography,SEC)是基于大小而非分子量实现分离大分子。该技术应用填充多孔聚合物微球的柱子,分子根据其直径通过微球,半径小的分子需要更长的时间才能通过色谱柱的孔隙迁移,而大分子则从色谱柱中更早地洗脱。尺寸排阻色谱可以精确分离大小分子。此外,可以将不同的洗脱溶液应用于该方法。与离心方法相比,色谱分离已被证明具有更多优势,因为通过色谱分离的外泌体不受剪切力的影响,这可能会改变囊泡的结构。目前,SEC是一种普遍接受的分离血液和尿液中外泌体的技术。不过,该方法耗时较长,不适合大量样本处理。机械力或者吐温-20等化学添加物将会破坏外泌体等,因此发表文章时易受质疑。昆明外泌体提取试剂供应商
外泌体提取:小分子可进入凝胶中绝大部分孔洞,在柱中受到更强地滞留,更慢地被洗脱出。南京外泌体提取试剂供应商
外泌体的提取方法:1、磁珠免疫法。外泌体表面有其特异性标记物(如CD63、CD9蛋白),用包被抗标记物抗体的磁珠与外泌体囊泡孵育后结合,即可将外泌体吸附并分离出来。磁珠法具有特异性高、操作简便、不影响外泌体形态完整等优点,但是效率低,外泌体生物活性易受pH和盐浓度影响,不利于下游实验,难以普遍普及。2、多聚物沉淀法。聚乙二醇(PEG)为常用的多聚物,可与疏水性蛋白和脂质分子结合共沉淀,早先应用于从血清等样本中收集病毒,现在也被用来沉淀外泌体,其原理可能与竞争性结合游离水分子有关。利用PEG沉淀外泌体存在不少问题:比如纯度和回收率低,杂蛋白较多(假阳性),颗粒大小不均一,产生难以去除的聚合物,机械力或者吐温-20等化学添加物将会破坏外泌体等。南京外泌体提取试剂供应商
外泌体与神经退行性疾病:外泌体可能促进或限制大脑中未折叠和异常折叠的蛋白质的聚集。AD病人脑脊液外泌体中均可检测到Tau和Aβ蛋白。类似的现象也在PD和ALS疾病中发现。PD病人脑脊液外泌体可检测到α-synuclein,ALS病人外泌体中也可以检测到SOD1或TDP-43。外泌体与疾病诊断(应用潜能):外泌体生成机制表明,通过分析外泌体的组分,可以帮助识别其来源的细胞类型。这一特性已被应用于开发心血管疾病,神经系统疾病和一些病症的分子诊断方法,也在肝肾肺相关疾病中进行研发测试。将沉淀物用PBS缓冲液进行悬浮,使外泌体悬浮于液体上层外泌体生物活性易受pH和盐浓度影响,不利于下游实验,难以普遍普...
- 宁波正规外泌体提取试剂报价 2026-02-24
- 深圳外泌体提取试剂厂家 2026-02-24
- 芜湖外泌体提取试剂销售厂家 2026-02-24
- 珠海外泌体提取试剂报价 2026-02-24
- 南昌正规外泌体提取试剂进货价 2026-02-24
- 重庆正规外泌体提取试剂服务电话 2026-02-24
- 武汉外泌体提取试剂服务电话 2026-02-24
- 济南正规外泌体提取试剂直销厂家 2026-02-24
- 无锡外泌体提取试剂厂家批发价 2026-02-24
- 重庆外泌体提取试剂平均价格 2026-02-24
- 石家庄正规外泌体提取试剂厂家现货 2026-02-14
- 温州正规外泌体提取试剂哪家便宜 2026-02-14
- 上海外泌体提取试剂直销厂家 2026-02-14
- 贵阳外泌体提取试剂推荐厂家 2026-02-13
- 贵阳外泌体提取试剂销售厂家 2026-02-13
- 宁波正规外泌体提取试剂销售厂家 2026-02-13


- 杭州正规RNA提取试剂哪家便宜 02-25
- 济南正规外泌体提取试剂产品介绍 02-25
- 太原鼠尾胶原厂家直销 02-25
- 深圳正规细胞外基质胶直销厂家 02-25
- 南昌RNA提取试剂销售厂家 02-25
- 成都正规RNA提取试剂直销价 02-25
- 苏州RNA提取试剂哪里买 02-25
- 青岛细胞外基质胶平均价格 02-25
- 珠海细胞外基质胶服务电话 02-25
- 石家庄正规无血清细胞冻存液平均价格 02-24