- 品牌
- 同顺生物
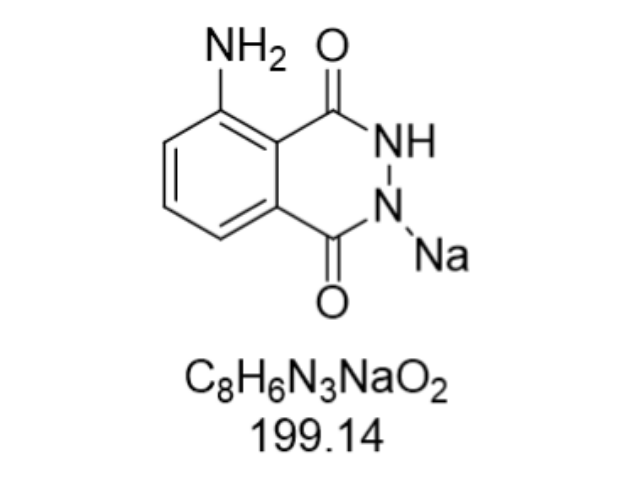
从物理化学性质看,鲁米诺钠盐表现出优异的稳定性与溶解特性。其熔点达319-320℃,沸点621.9℃(760 mmHg),密度1.433 g/cm³,这些参数表明该物质在高温环境下仍能保持结构完整。在溶解性方面,室温下可溶于水(50 mg/mL),超声处理后溶解度提升至100 mg/mL,这一特性使其在配置HRP底物液时无需有机溶剂辅助,明显降低了实验操作的复杂性。2024年某生物技术公司开展的比较实验显示,采用鲁米诺钠盐配置的化学发光底物,其信号稳定性(CV值<3%)优于鲁米诺自由酸(CV值>8%),这得益于钠盐形式减少了溶液中质子化竞争反应。储存条件方面,推荐在2-8℃避光密封保存,在此条件下产品纯度(≥99%)可维持24个月以上,而室温储存会导致每月约0.5%的降解率,主要降解产物为3-氨基邻苯二甲酸,该物质会竞争性消耗氧化剂从而降低发光效率。部分化学发光物可重复利用,通过特定处理恢复其发光性能。乌鲁木齐腔肠素
除了作为法医学上的隐形血迹揭示者,鲁米诺还因其独特的化学发光性质在生物分析和传感器技术中占据一席之地。科研人员通过设计复杂的分子结构或利用纳米技术,将鲁米诺与其他功能性材料结合,开发出高灵敏度和选择性的化学发光传感器,用于检测生物体内的活性氧物种、金属离子、药物分子等。这些传感器不仅提高了检测的准确性和效率,还为疾病诊断、环境监测和药物筛选等领域带来了进步。鲁米诺的发光反应还可以通过调控反应条件实现信号放大,进一步提高了检测灵敏度,使得微量分析成为可能。因此,尽管鲁米诺的发现距今已有多年,但其应用潜力仍在不断被挖掘,持续在科学研究和实际应用中发光发热。乌鲁木齐腔肠素化学发光物1,2-二氧环乙烷,通过结构修饰可调节发光动力学。
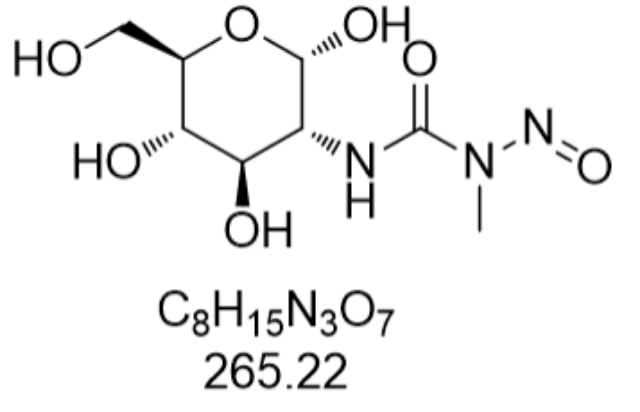
在糖尿病动物模型构建领域,链脲菌素已成为不可替代的标准工具。其致糖尿病作用具有明显的种属特异性:大鼠和小鼠对链脲菌素高度敏感,而豚鼠和人类则表现出天然抵抗。这种选择性源于GLUT2转运蛋白在胰岛β细胞中的表达差异——只有表达GLUT2的细胞才能高效摄取链脲菌素。实验证明,单次大剂量注射(65-70mg/kg体重)可快速破坏80%以上的β细胞,导致胰岛素分泌缺乏,模拟人类1型糖尿病病理特征;而多次小剂量注射(30mg/kg×5次)则通过T细胞介导的免疫反应渐进性破坏β细胞,更接近2型糖尿病的发病机制。配合高脂高糖饮食预处理,可构建出胰岛素抵抗与β细胞功能衰竭并存的2型糖尿病模型。值得注意的是,模型成功率与操作细节密切相关:禁食12小时以上可增强药物渗透性,推注速度需控制在30秒内完成以避免溶液降解,补救注射(10-20mg/kg)可在初次注射后72小时实施以提高成模率。这些参数的精确控制使链脲菌素模型在药物筛选、病理机制研究中保持不可替代的地位。
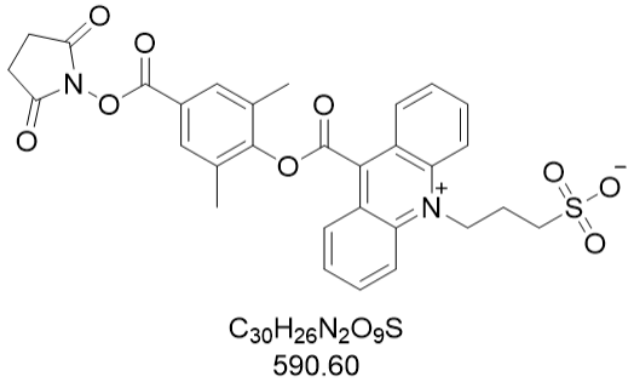
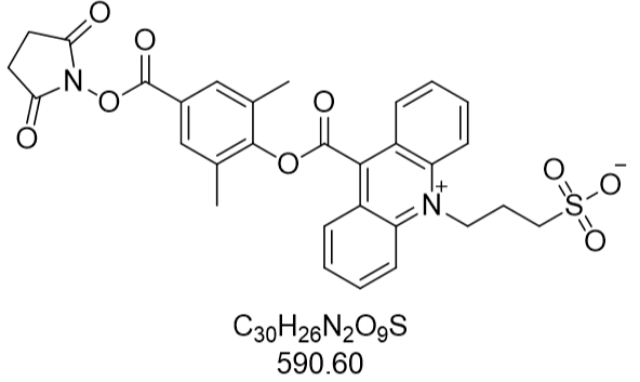
APS-5化学发光底物(CAS: 193884-53-6)的重要性能优势集中体现在其超高的检测灵敏度上。作为基于9,10-二氢吖啶结构的化合物,APS-5在碱性磷酸酶(ALP)催化下可检测到低至1×10⁻¹⁹ mol(约0.01 pg)的酶分子浓度,这一数值远超传统化学发光底物。其分子结构中的氯苯硫代磷酰氧亚甲基基团与吖啶环形成稳定共轭体系,在ALP水解磷酸基团后,生成的不稳定中间体可在数秒内分解并释放光子,光子释放效率较上一代底物提升3-5倍。实验数据显示,在TSH(促甲状腺物质)标记物检测中,APS-5的相对发光强度(RLU)可达3,000,000以上,而空白对照的RLU值低于1,000,信噪比超过3,000:1。这种灵敏度使得APS-5在疾病标志物检测中可识别皮克级浓度的抗原,为早期疾病筛查提供关键技术支撑。此外,其检测下限突破传统底物的纳克级限制,在基因芯片研究中可实现单分子级别的酶活性定位,推动高通量测序技术的精度提升。吖啶酯作为高效化学发光物,常用于免疫分析中标记抗体分子。
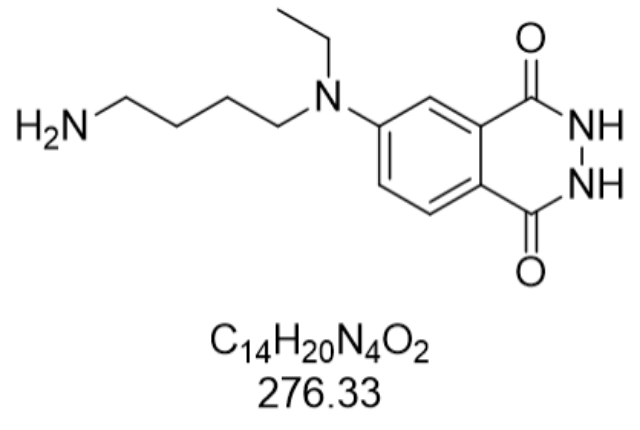
从应用场景看,鲁米诺钠盐的化学发光特性已渗透至多学科交叉领域。在生物医学研究中,该试剂被用于检测细胞活性氧(ROS)水平,通过发光强度量化氧化应激程度,为神经退行性疾病研究提供量化指标。环境监测领域,其与辣根过氧化物酶(HRP)联用可检测水体中痕量有机污染物,检测限低至0.1ppb。在法医毒理学中,鲁米诺钠盐不仅能检测血液,还可通过特定氧化剂组合识别精斑、唾液等生物痕迹。值得关注的是,该试剂在化学示踪领域展现出独特优势,通过标记特定分子实现成像,为疾病转移机制研究提供可视化工具。其发光效率受pH值影响明显,在pH8-10的碱性环境中发光强度达到峰值,这一特性被用于构建pH响应型智能检测系统。吖啶酯化学发光物反应本底低,适合超微量生物标志物检测。N-(4-氨丁基)-N-乙基异鲁米诺供应公司
化学发光物的发光颜色可通过改变分子结构进行调控,满足不同需求。乌鲁木齐腔肠素
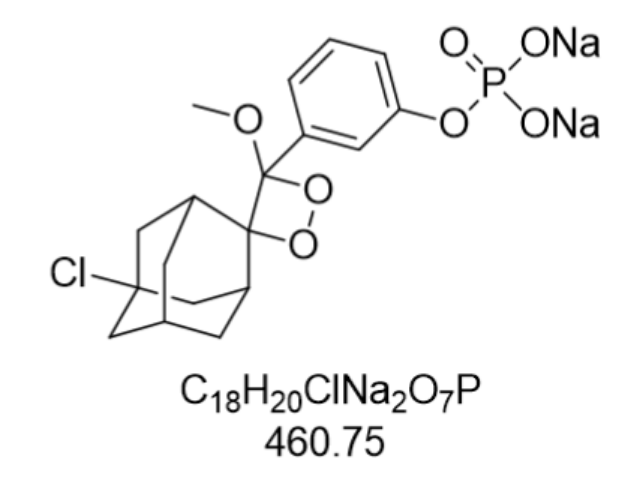
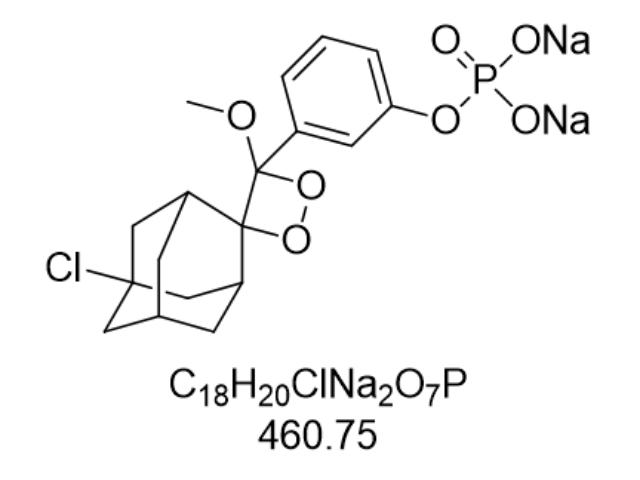
从分子机制层面分析,CSPD的性能优势源于其独特的化学结构设计。螺环金刚烷部分通过空间位阻效应,有效抑制了非酶促水解反应,而二氧杂环丁烷环的张力能则降低了酶促裂解的活化能。当碱性磷酸酶作用于磷酸酯基团时,分子内发生重排,释放出激发态中间体,该中间体通过化学发光途径衰变,产生波长为470 nm的蓝光。这一发光过程无需额外激发光源,避免了荧光淬灭和光漂白问题,同时其量子产率(约0.15)明显高于传统过硫酸盐体系。结构优化还体现在甲氧基的引入上,该基团通过氢键作用稳定了酶-底物复合物,使催化效率(kcat/Km)达到1.2×10⁶ M⁻¹s⁻¹,较无取代类似物提高了2倍。这种结构-活性关系的精确调控,使得CSPD在复杂生物样本中仍能保持高特异性识别能力。乌鲁木齐腔肠素
腔肠素不仅在生物学研究中占据重要地位,在医学领域也展现出巨大潜力。作为一种内源性,腔肠素(此处指具有生理活性的多肽,与上述发光化合物同名但不同物质)由胃部的G细胞分泌并释放到血液中,主要作用于胃壁上的壁细胞,刺激胃酸和胃黏液的分泌,加速胃肠道蠕动,延缓胃排空,从而协调整个消化系统的功能。这一生理作用使得腔肠素在胃病诊疗中具有重要价值。通过检测腔肠素水平的变化,医生可以评估患者的胃酸分泌情况,进而判断是否存在胃酸过多引起的胃溃疡、胃食管反流等疾病。腔肠素还可以作为研发药物的靶点或指标之一,针对其作用机制开发相关药物,如抑制胃酸分泌的药物、调节胃肠道蠕动的药物等。随着研究的深入,腔肠素的应用范围还...
- CDP-STAR化学发光底物生产商家 2026-03-17
- 石家庄三联吡啶氯化钌六水合物 2026-03-17
- 银川化学发光物 2026-03-16
- 哈尔滨氨己基乙基异鲁米诺 2026-03-16
- 双-(4-甲基伞形酮)磷酸酯经销商 2026-03-15
- 湖南鲁米诺 2026-03-15
- 南京化学发光物 2026-03-15
- 浙江9-吖啶羧酸 2026-03-14
- 黑龙江鲁米诺 2026-03-14
- 鲁米诺钠盐厂家供应 2026-03-14
- 兰州异鲁米诺 2026-03-11
- 9-吖啶羧酸 2026-03-11
- 青海APS-5化学发光底物 2026-03-11
- 四川4-甲基伞形酮酰磷酸酯 2026-01-25
- 4-甲基伞形酮磷酸酯 二钠盐现货 2026-01-25
- 无锡吖啶酸丙磺酸盐 2026-01-24


- CDP-STAR化学发光底物生产商家 03-17
- 上海化妆品添加剂厂家直销 03-17
- 上海甲萘醌-4生产公司 03-17
- 石家庄三联吡啶氯化钌六水合物 03-17
- 苏州胆固醇硫酸酯钾盐价格 03-17
- 内蒙古德兰佐米 03-16
- 广东2-溴-1 03-16
- 宁夏紫杉醇 03-16
- 银川化学发光物 03-16
- 哈尔滨氨己基乙基异鲁米诺 03-16