J774A.1小鼠单核巨噬细胞是一种来源于小鼠的单核巨噬细胞系,广泛应用于免疫学和炎症研究领域。该细胞系具有典型的巨噬细胞特性,能够执行吞噬、抗原呈递以及分泌多种细胞因子等功能。J774A.1细胞在体外培养中表现出稳定的增殖能力和功能活性,常用于研究免疫应答、炎症反应以及巨噬细胞与病原体的相互作用。由于其对人巨噬细胞功能的良好模拟,J774A.1细胞成为探索先天免疫、细胞吞噬机制以及相关信号通路的重要模型。此外,J774A.1细胞在药物筛选、毒性测试以及免疫调节研究中也发挥了积极作用。由于其易于培养和多功能性,J774A.1小鼠单核巨噬细胞为免疫学和炎症研究提供了重要的实验工具,为深入理解巨噬细胞行为和相关免疫机制提供了支持。细胞膜上的受体接收外界信号,触发细胞反应。CCRF-CEM急性淋巴细胞白血病T淋巴细胞
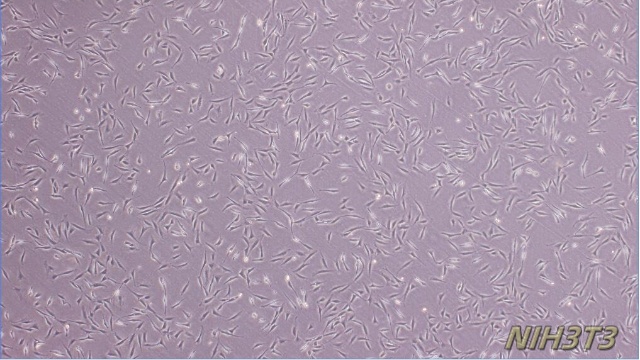
MLE-12细胞是一种来源于小鼠肺组织的上皮细胞系,具有典型的肺泡Ⅱ型上皮细胞特征。这类细胞在体外培养中能够表达表面活性蛋白C(SP-C)等特异性标志物,是研究肺表面活性物质代谢及肺泡上皮功能的常用模型。MLE-12细胞保持了一定的分化能力,可用于模拟肺泡上皮的屏障特性和物质转运功能。通过研究MLE-12细胞,可以深入探讨肺上皮细胞在维持肺泡稳态中的分子机制,包括表面活性物质合成与分泌、离子通道调控以及细胞间连接的形成。该细胞系对氧化应激等外界刺激表现出敏感响应,为研究肺上皮损伤修复机制提供了便利工具。MLE-12细胞还被用于探索上皮细胞与免疫细胞的相互作用,在呼吸系统基础研究中具有重要价值,为肺部生理和病理机制研究提供了可靠的体外实验平台。小鼠骨髓嗜碱细胞细胞内的内质网参与蛋白质和脂质的合成。
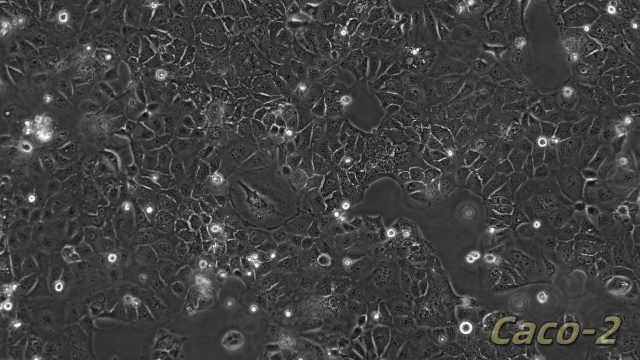
HMC3人小胶质细胞是一种来源于人脑的小胶质细胞系,主要用于神经免疫学和***系统研究。该细胞系具有小胶质细胞的典型特性,能够执行免疫监视、吞噬功能以及分泌多种神经免疫调节因子。HMC3细胞在体外培养中表现出稳定的增殖能力和功能活性,常用于研究神经炎症、免疫应答以及小胶质细胞与神经元的相互作用。由于其对人小胶质细胞功能的良好模拟,HMC3细胞成为探索神经免疫调控、细胞吞噬机制以及相关信号通路的重要模型。此外,HMC3细胞在药物筛选、神经退行性研究以及***系统疾病机制探索中也发挥了积极作用。由于其易于培养和多功能性,HMC3人小胶质细胞为神经免疫学和***系统研究提供了重要的实验工具,为深入理解小胶质细胞行为和相关神经免疫机制提供了支持。
ST细胞(SwineTestiscells,猪睾丸细胞)是一种来源于猪睾丸组织的贴壁生长细胞系,因其稳定的增殖特性和易转染性,被广泛应用于病毒培养、基因工程及疫苗研发等领域。在病毒学研究中,ST细胞对多种猪源病毒(如猪圆环病毒、猪细小病毒)高度敏感,常用于病毒的分离、扩增及疫苗生产。由于其与人类细胞在某些病毒受体上的相似性,ST细胞也被用于部分人畜共患病病毒的研究,如**戊型肝炎病毒(HEV)**的体外复制机制分析。在分子生物学领域,ST细胞因其高效的蛋白表达能力和较低的支原体污染风险,常作为重组蛋白生产的宿主细胞。此外,ST细胞还可用于基因编辑技术(如CRISPR-Cas9)的验证实验,或作为转基因动物研究的体外模型。ST细胞在培养时需使用含10%胎牛血清的DMEM培养基,并保持37℃、5%CO₂的恒温环境。其形态呈典型的上皮样贴壁生长,传代稳定性良好,是兽医学和生物技术研究中重要的工具细胞之一。细胞分裂是生物体生长和繁殖的基础。
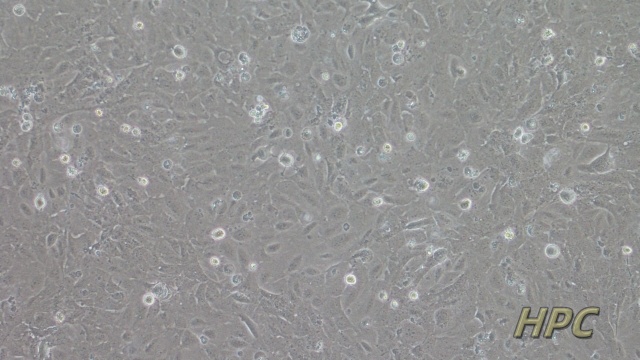
HK-2人肾皮质近曲小管上皮细胞是一种永生化的人肾皮质近曲小管上皮细胞系,来源于正常成人肾脏组织,经HPV16E6/E7基因转染获得永生化特性。该细胞保留了近曲小管上皮细胞的许多特性,如表达刷状缘酶(如碱性磷酸酶)和转运蛋白(如钠-葡萄糖共转运蛋白SGLT2),因此广泛应用于肾脏生理和病理研究,特别是急性肾损伤(AKI)、慢性肾脏病(CKD)和药物性肾毒性等疾病的体外模型构建。HK-2细胞在肾脏疾病机制研究中具有重要价值。例如,通过暴露于肾毒性物质(如顺铂、庆大霉素)或高糖环境,可以模拟药物性肾损伤和糖尿病肾病的病理过程,研究其分子机制及潜在干预措施。此外,HK-2细胞还被用于研究肾脏纤维化、氧化应激和炎症反应在慢性肾脏病进展中的作用,以及肾脏上皮细胞在缺血再灌注损伤中的反应。在培养方面,HK-2细胞通常采用含10%胎牛血清的DMEM/F12培养基,需在37℃、5%CO₂环境下进行。由于其易于培养和高重复性的特点,HK-2细胞成为研究肾脏疾病机制和药物筛选的重要工具。通过基因编辑技术(如CRISPR-Cas9)和转录组分析,科学家能够深入探索肾脏上皮细胞在疾病发***展中的作用,并开发新的***策略。线粒体是细胞的能量工厂,负责ATP的合成。HSAS2人皮肤成纤维细胞
细胞核内的核仁参与核糖体的合成。CCRF-CEM急性淋巴细胞白血病T淋巴细胞
L6大鼠成肌细胞是一种来源于大鼠骨骼肌的细胞系,广泛应用于肌肉生物学和代谢研究领域。该细胞系由Yaffe和Saxel于1977年建立,具有典型的成肌细胞特性,能够在低血清条件下分化为多核肌管,模拟骨骼肌的形成过程。L6细胞在分化过程中会表达肌肉特异性标志物,如肌球蛋白和肌酸激酶,因此常被用于研究肌肉分化机制及肌肉特异性基因的功能调控。此外,L6细胞对胰岛素敏感,能够响应胰岛素刺激并调节葡萄糖摄取,使其成为研究葡萄糖代谢、胰岛素信号通路以及肌肉相关代谢疾病的理想模型。在实验中,L6细胞通常通过优化培养条件(如使用2%马血清)诱导分化,以满足不同研究需求。由于其易于培养和高分化效率,L6细胞在药物筛选、能量代谢研究以及肌肉功能调控等领域发挥了重要作用。总之,L6大鼠成肌细胞因其独特的分化能力和代谢特性,为肌肉生物学和相关代谢研究提供了重要的实验工具。CCRF-CEM急性淋巴细胞白血病T淋巴细胞