在干细胞医治领域, 某些疾病靠单纯的细胞替代并不能取得满意效果。利用逆转录病毒和慢病毒将外源目的基因整合到干细胞基因组,对基因功能缺失的遗传病具有良好疗效,但也存在一定致瘤风险。相比之下,CRISPR/Cas9基因编辑技术能够精确实现基因敲入、敲除及碱基修复。因此, 采用CRISPR/Cas9基因编辑技术对干细胞进行基因改造,不仅能够增加干细胞医治的疾病范围,也能更大程度地保证疗效的安全性。目前,CRISPR/Cas9在干细胞医治领域发挥着重要作用,同时更多由CRISPR/Cas9编辑的干细胞药物正在开发中。M-SAN HQ ELISA kit具有高精确度及高准确度。广东生理盐条件中盐核酸酶70950
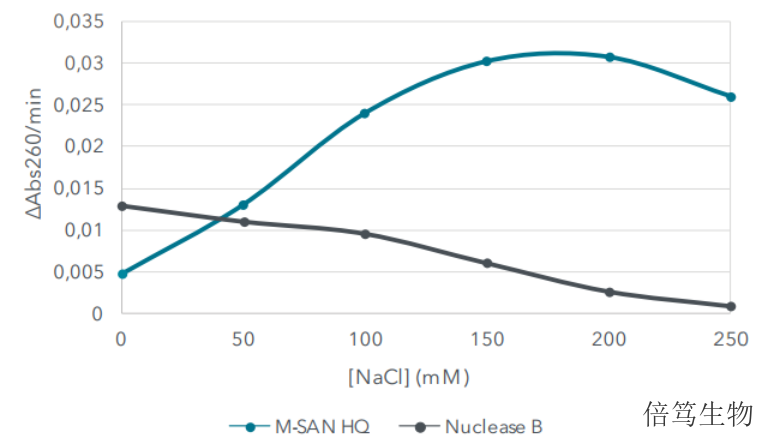
文章作者对酶法去除dsDNA进行了优化研究,两种酶浓度梯度为25U/ml、50U/ml及100U/ml,Mg2+浓度为5mM,通过PicoGreen检测dsDNA含量。结果发现,25U/ml的M-SAN HQ中盐核酸酶对dsDNA去除效果明显优于100U/ml的Benzonase。此外,在酶切反应速度方面,M-SAN HQ有更明显的优势,——在低浓度底物dsDNA(如20ng/ml)条件下,50U/ml的M-SAN HQ在5分钟内将dsDNA降解到2ng/ml左右;而50U/ml的Benzonase在30分钟孵育消化后,dsDNA浓度依然是12ng/ml左右。青海生理盐条件中盐核酸酶70950-160M-SAN HQ中盐核酸酶用在生产工艺流程中,在生理盐条件下去除双链及单链的DNA及RNA。

ArcticZymes Technologies于2019年推出了M-SAN HQ中盐核酸酶,2021年推出对应的M-SAN HQ ELISA kit。该试剂盒原理是采用双抗夹心法定量检测各种生物制品的中间品、半成品和成品中M-SAN HQ中盐核酸酶的残留含量,特异性的anti-M-SAN作为捕获抗体偶联在孔板上,辣根过氧化酶HRP标记anti-M-SAN作为检测抗体,TMB是检测反应底物。该试剂盒特异识别M-SAN HQ中盐核酸酶,对其它核酸酶没有特异性结合。它的定量范围是0.12-7.5ng/ml;12*8strips的设计规格,使用灵活,更能降低使用成本。
ArcticZymes Technologies推出了SAN HQ高盐核酸酶和M-SAN HQ中盐核酸酶,为生物工艺领域提供了革新性、更高效的方案来解决大规模生产中核酸残留问题。此前,受限于盐浓度和核酸酶活性的负调控效应,行业在核酸残留去除效果和酶成本之间寻找平衡,更多的是让工艺选择适应酶。此后,行业可以根据工艺具体需求而选择更合适的酶产品,既能达到理想的去除效果,又能轻松控制酶用量及综合成本,真正实现让酶适应工艺选择。SAN HQ和M-SAN HQ为行业提供更高效率的解决方案。相比全能核酸酶,M-SAN HQ中盐核酸酶能将HCD酶切成更小片段,破坏核小体结构。
市售的M-SAN HQ中盐核酸酶有三个规格,分别是25kU、500kU及5MU,分别满足研发初期及大规模生产各阶段的要求。通过SDS-PAGE检测蛋白纯度在99%以上。基于ArcticZymes Technologies的30年的酶学开发及大规模生产经验,M-SAN HQ的生产体系稳定,产品纯度高,批次一致性好,无蛋白酶活性。厂家开发出特异的缓冲液体系,使M-SAN HQ保存起来更加稳定,-15℃ - -30℃条件下保存4年没有活性下降。研究数据表明,经过5-6次的反复冻融,M-SAN HQ中盐核酸酶活性没有明显变化。生理盐浓度下,M-SAN HQ中盐核酸酶性能优于常用核酸酶。广东M-SAN中盐核酸酶70950-160
M-SAN HQ ELISA kit检测产品灵敏度高,定量范围为0.12-7.5ng/ml。广东生理盐条件中盐核酸酶70950
经典的慢病毒载体(LV)的生产工艺如下,——三质粒系统瞬时转染HEK293细胞系,转染24小时后LV由转染阳性细胞生产并排出到培养上清液中;收获上清培养液后,加入核酸酶去除HCD污染,通过澄清步骤去除大的细胞碎片等杂质;下游纯化步骤分离LV载体,纯化方法包括切向流过滤TFF、色谱纯化及超速离心;纯化后的LV病毒颗粒经过无菌过滤,更换到优化后的配方中,灌装并冷冻保存。每批Car-T生产时取对应量的LV病毒,切忌反复冻融,否则LV病毒会失活。广东生理盐条件中盐核酸酶70950
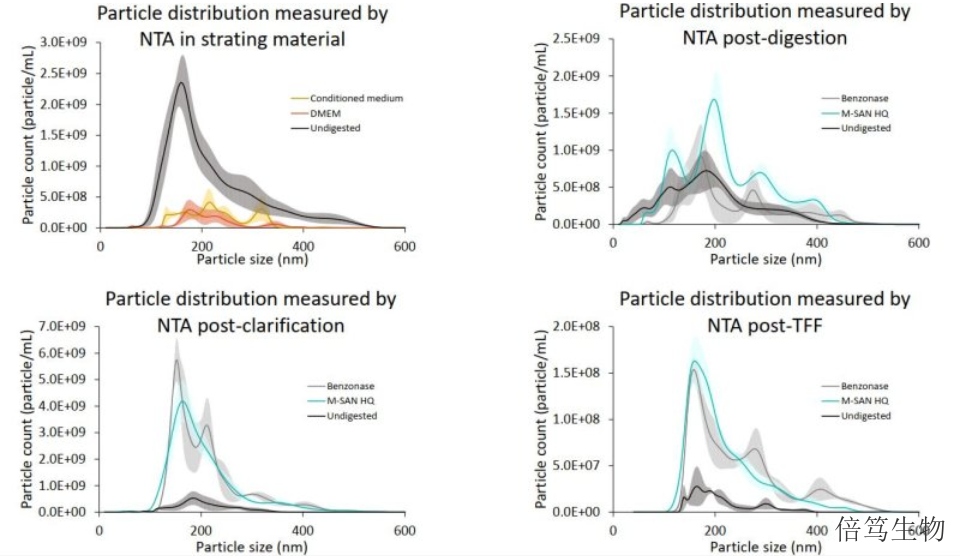
文章作者按照经典的慢病毒载体生产流程操作,在融化、核酸酶消化、澄清、超滤等步骤留样,分别检测dsDN...
【详情】除了获得载体的滴度及产量,生产慢病毒更关心的指标主要是各种污染物的去除。总DNA污染的去除百分比在9...
【详情】细胞基因药物领域的进展使得对高质量基因转移技术的需求急剧增加,包括高质量慢病毒载体(LV)的大规模生...
【详情】细胞基因药物的基因递送有病毒及非病毒两种方式,其中病毒递送更为常用。在病毒递送路径中,腺相关病毒(A...
【详情】大规模生产阶段,AAV/LV载体生产流程跟抗体、疫苗类药物的生产类似,主要包含上游培养、下游纯化及制...
【详情】核酸酶活性受到很多因素影响,如盐浓度、pH、底物、温度等。因此,不同客户、不同项目中核酸酶的使用条件...
【详情】病毒载体作为细胞药物生产的关键原材料,直接关系到细胞产品质量。载体质量的控制和工艺稳定性和批间一致性...
【详情】在生物工艺流程中,需要使用核酸酶去除终产品中的核酸污染,而核酸酶作为外源成份,也需要在生产流程中去除...
【详情】残留的宿主DNA是生产中产生的杂质,其存在潜在的致瘤性、传染性和免疫原性等风险。相关研究表明,基因的...
【详情】慢病毒载体既可以转导分裂细胞也可以转导非分裂细胞,被认为是安全的,并且可以提供长期的转基因表达,是目...
【详情】文章作者对酶法去除dsDNA进行了优化研究,两种酶浓度梯度为25U/ml、50U/ml及100U...
【详情】在传统生物技术行业(如抗体、疫苗领域)使用的下游纯化工艺步骤,已经用于慢病毒的大规模下游处理。主要是...
【详情】